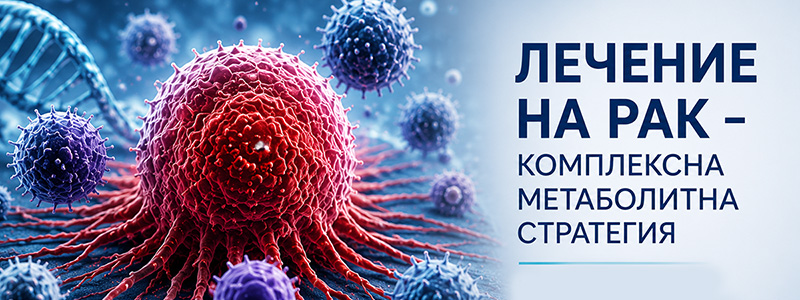
Прогресията на рака произтича от взаимодействието на три области: вътрешно метаболитно и сигнално пренареждане в туморните клетки, микросредови условия, поддържащи оцеляването и разпространението на тумора, и системна метаболитна дисфункция в организма на гостоприемника. Тези слоеве съвместно движат резистентността към лечение, имунното избягване и рецидива. Целенасочената метаболитна терапия (ЦМТ) е предложена като цялостна терапевтична рамка, предназначена едновременно да таргетира и трите области на раковата прогресия. ЦМТ насочва въздействието си към ключови метаболитни пътища, замесени в туморния растеж и оцеляване — като гликолиза, глутаминолиза, IGF-1/PI3K-AKT-mTOR, ангиогенеза, резистентност към апоптоза и Wnt/β-катенин сигнализиране — като същевременно нарушава микросредови фактори, включително туморна стволовост, метастази, ацидоза, хипоксия и хронично възпаление. На системно (гостоприемниково) ниво ЦМТ коригира метаболитни нарушения — включително хипергликемия, системно възпаление и кахексия — които създават благоприятна среда за туморна прогресия.
Терапевтичният модел интегрира множество интервенционни категории: диетични стратегии и гладуване, преназначени фармакологични средства, нутрицевтици, основни витамини и минерали. Допълнителни компоненти включват терапии, модулиращи кислород и редокс-баланса, и мерки за оптимизиране на начина на живот. Тази статия очертава биологичното обосноване на ЦМТ и предлага рамка на системно ниво за прилагане на координиран метаболитен натиск с цел подобряване на терапевтичния отговор, удължаване на преживяемостта и предоставяне на пациентите с рак на по-трайна перспектива за контрол на заболяването и ремисия.
През последните десетилетия все повече данни преосмислят рака не само като генетично заболяване, а фундаментално като метаболитна болест. Оригиналните наблюдения на Варбург са подчертали предпочитанието на туморните клетки към аеробна гликолиза дори при наличие на достатъчно кислород. По-нататъшната работа на Сейфрид и други разширява тази концепция, акцентирайки върху централната роля на нарушения глюкозен и глутаминов метаболизъм като основни биоенергетични двигатели на злокачествеността. По-широко, раковите клетки интегрират променено усвояване на субстрати, редокс-контрол, митохондриално препрограмиране и сигнализиране на растежни фактори в координирана метаболитна мрежа, поддържаща пролиферация, инвазия и оцеляване при стрес.
Туморното поведение допълнително се определя от микросредата му. Отсечки от туморни стволови клетки, метастатични програми, лактат-задвижена ацидоза, хипоксия, стромални взаимодействия и хронично възпаление съвместно определят имунната достъпност, метастатичния потенциал и резистентността към лечение. Тези микросредови двигатели действат наред с вътрешните метаболитни пътища, образувайки тясно свързана екосистема, а не чисто клетъчно-автономен процес.
В същото време много пациенти са изправени пред системни метаболитни дисфункции, създаващи поддържаща среда за раковата прогресия. Хроничното възпаление, хипергликемията и анормалните кръвни показатели са свързани с по-лоши резултати и увеличена смъртност от рак. Тези аномалии на ниво гостоприемник отслабват имунното наблюдение, усилват про-туморното сигнализиране (напр. чрез IGF-1/PI3K-AKT-mTOR) и улесняват кахексията и непоносимостта към лечение.
В този контекст предлагаме целенасочената метаболитна терапия (ЦМТ) като комплексна терапевтична рамка, която едновременно адресира туморно-вътрешните механизми и метаболитните уязвимости на гостоприемника. ЦМТ се основава на два взаимосвързани стълба: блокиране на доминиращите метаболитни и сигнални центрове (включително гликолиза, глутаминолиза, ангиогенеза/HIF сигнализиране, IGF-1/PI3K-AKT-mTOR, Wnt/β-катенин, апоптотична резистентност и имунно избягване, туморна стволовост, метастази, киселинност, хипоксия и възпаление); и възстановяване на метаболитното здраве на пациента чрез корекция на системни дисфункции, подхранващи туморния растеж.
За да операционализира тази концепция, ЦМТ интегрира: диетични стратегии и гладуване (кетогенни диети, интермитентно и продължително гладуване); преназначени лекарства с определени метаболитни и сигнални ефекти (ивермектин, фенбендазол и мебендазол, итраконазол, метформин, налтрексон в ниска доза, бебешки аспирин); многоцелеви нутрицевтици (куркумин, берберин, тимохинон, омега-3 мастни киселини, модифициран цитрусов пектин, β-глюкан-съдържащи лечебни гъби, лактоферин); витамини и ключови минерали с документирани антиракови или защитни за гостоприемника роли (витамин D, цинк, селен, магнезий); допълнителни редокс и кислородни терапии (канабидиол, натриев бикарбонат, хипербарен кислород); и оптимизиране на начина на живот (физически упражнения, регулиране на съня, структурирано управление на стреса).
Тази статия синтезира механистичното обосноване и подкрепящите доказателства за интервенциите на ЦМТ в единна метаболитна рамка. Представя схема, базирана на пътища, за изграждане на рационални, нискотоксични, многоцелеви терапевтични протоколи. Интервенциите са съобразени с конкретни туморни пътища, микросредови двигатели и метаболитни дисфункции на гостоприемника.
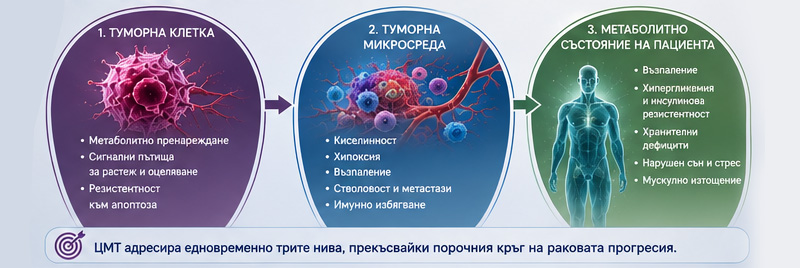
Пътища за туморен растеж и сигнализиране
Раковите клетки оцеляват и се размножават чрез пренареждане на метаболитните и сигналните си пътища. Тези мрежи осигуряват постоянно гориво, суровини за нови клетки и защита срещу сигналите за смърт и имунните атаки. За разлика от здравите клетки, разчитащи на балансирано производство на енергия, туморите показват екстремна метаболитна пластичност: ако един растежен маршрут бъде блокиран, незабавно се активира друг. Тази адаптивност обяснява защо конвенционалните терапии често се провалят.
Сред многото описани промени, няколко се открояват като най-универсалните двигатели на раковия растеж: гликолиза, глутаминолиза, ангиогенеза, апоптотична резистентност и имунно избягване. Тези основни механизми представляват главните мишени на ЦМТ.
Гликолиза и ефектът на Варбург
Една от най-старите и добре документирани особености на рака е неговото необичайно високо потребление на глюкоза. Туморните клетки могат да използват 10-15 пъти повече глюкоза от нормалните клетки за поддържане на бързия растеж и делене. В допълнение, много ракови заболявания показват значителна свръхекспресия на инсулинови рецептори, особено на изоформата IR-A, правейки ги свръхчувствителни към инсулина и IGF-1 сигнализирането. Това осигурява непрекъснато поемане на глюкоза дори при ниски нива на хранителни вещества.
Вместо да разчитат на ефективното митохондриално производство на енергия, раковите клетки преимуществено превръщат глюкозата в лактат дори при наличие на кислород — класическият ефект на Варбург. Тази промяна не е само за енергия: тя доставя строителни блокове за ДНК, протеини и липиди, докато лактатът подкислява околната тъкан, помагайки на туморите да нахлуват и да потискат имунните клетки.
Високата гликолитична активност е характерна за всички ракови заболявания и представлява основата на образната диагностика с флуородеоксиглюкоза (FDG)-позитронно-емисионна томография (PET), при която поемането на глюкоза осветлява туморите в цялото тяло. Клиничните проучвания показват, че повишените маркери на гликолизата, като GLUT1 и LDH-A, са силно свързани с агресивно заболяване и лоша преживяемост.
Глутаминолиза
Глутаминът служи като второто основно гориво за много тумори — явление, нарядко наричано глутаминова зависимост. След поглъщане, глутаминът се превръща в глутамат и след това в α-кетоглутарат, попълвайки интермедиерите на цикъла на трикарбоксилните киселини (ЦТК) за поддържане на производството на енергия и анаболизма. Той осигурява азот и въглерод за синтеза на нуклеотиди и аминокиселини, директно подкрепяйки бързото клетъчно деление. Освен това глутаминът е ключов предшественик на глутатиона и другите антиоксидантни защити, помагайки на злокачествените клетки да понасят оксидативен и метаболитен стрес. Глутаминазата (GLS1), катализираща първата стъпка на този път, е нерядко свръхрегулирана при рак.
Ангиогенеза и хипоксичен отговор
Тъй като туморите растат отвъд границите на простата дифузия, те се нуждаят от нови кръвоносни съдове за доставка на кислород и хранителни вещества. Това се постига чрез ангиогенеза, задвижвана в голяма степен от хипоксия-индуцирана стабилизация на HIF-1α и последващата индукция на проангиогенни гени като VEGF. HIF-1α също засилва гликолитичния капацитет чрез регулиране нагоре на глюкозните транспортери и гликолитичните ензими, свързвайки хипоксията директно с метаболитното препрограмиране.
Свръхекспресията на HIF-1α е документирана при много човешки ракови заболявания и техните метастази и е свързана с по-агресивно заболяване и по-лоши резултати.
Апоптотична резистентност
Злокачествените клетки трябва да избягват програмираната клетъчна смърт, за да оцеляват и да се размножават. При нормални условия апоптозата елиминира клетките с прекомерни ДНК увреждания или онкогенен стрес, поддържайки тъканната хомеостаза. Туморите нерядко накланят баланса на протеините от семейство BCL-2 към оцеляване, със свръхекспресия на антиапоптотични членове като BCL-2 и BCL-XL и намалена функция на проапоптотични регулатори като BAX и PUMA. Чрез предотвратяване на пермеабилизацията на външната митохондриална мембрана и активирането на каспазата, този дисбаланс позволява на раковите клетки да устояват на генотоксично увреждане и цитотоксични терапии.
Имунно избягване
Въпреки че имунната система може да открива и унищожава трансформирани клетки, клинично очевидните тумори са избягали от това наблюдение. Имунното избягване вече се признава като основна характеристика на рака и е тясно свързано с метаболитното пренареждане. В туморната микросреда раковите клетки се конкурират с Т-клетките за глюкоза и ключови аминокиселини, ограничавайки субстратите, необходими за ефективни имунни отговори. Натрупването на лактат и свързаната ацидоза допълнително потискат цитотоксичната Т-клетъчна активност и благоприятстват регулаторни или изтощени фенотипове. Много тумори също свръхрегулират имунни контролни лиганди като PD-L1, което инхибира Т-клетъчната функция и насърчава имунното избягване.
Пътят IGF-1/PI3K-AKT-mTOR
Инсулиновата и IGF-1 ос се сходят в пътя PI3K-AKT-mTOR — централен регулатор на клетъчния растеж, метаболизма и оцеляването. Активирането на PI3K и AKT засилва поемането на глюкоза, стимулира анаболния метаболизъм и осигурява силни антиапоптотични сигнали. По-надолу mTOR интегрира хранителните сигнали и тези на растежните фактори, за да задвижи синтеза на протеини и липиди, потискайки автофагията и позволявайки бързото разширяване на злокачествени клетъчни популации. Нарушаването на регулацията на този път е честo срещано при рак. Системни метаболитни състояния като затлъстяване и хиперинсулинемия могат допълнително да усилят IGF-1/PI3K-AKT-mTOR сигнализирането, директно свързвайки метаболизма на гостоприемника с туморната прогресия.
Пътят Wnt/β-катенин и други механизми
Друг основен сигнален маршрут при рака е пътят Wnt/β-катенин, управляващ клетъчната съдба, пролиферацията и стволовостта. В нормалните тъкани β-катениновата регулация е строга, но при тумори мутациите или абнормното Wnt активиране стабилизират β-катенина, позволявайки му да се натрупва в ядрото и да задвижва транскрипцията на онкогенни програми. Това насърчава неконтролирания растеж и поддържа туморните стволови клетки (ТСК), нерядко по-резистентни към терапия. Сигнализирането Wnt/β-катенин също допринася за имунното изключване; тумори с висока β-катенинова активност нерядко нямат Т-клетъчна инфилтрация и реагират слабо на имунотерапия.
Докато гликолизата, глутаминолизата, ангиогенезата, апоптотичната резистентност, имунното избягване, IGF-1/PI3K-AKT-mTOR и Wnt/β-катенин са доминиращите двигатели на растежа, раковата прогресия включва и много допълнителни пътища. Те включват Hedgehog и Notch сигнализирането, каскадата MAPK/ERK, MYC-задвижваното транскрипционно препрограмиране, NRF2-медиираните антиоксидантни отговори и загубата на туморни супресори като p53.
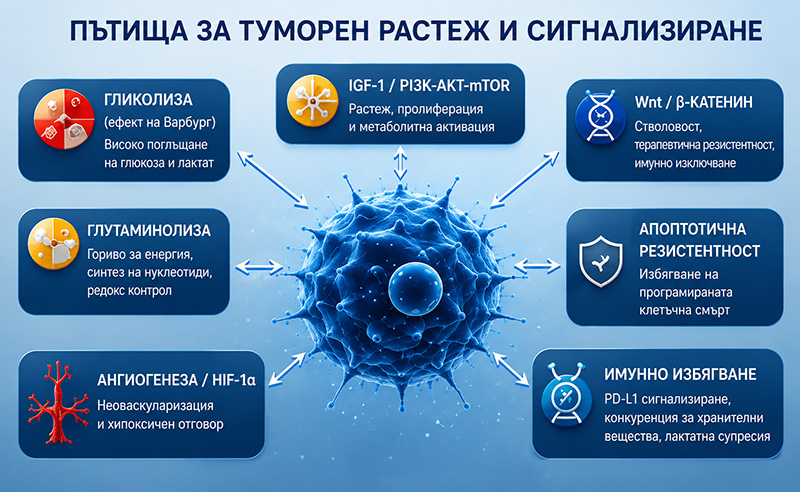
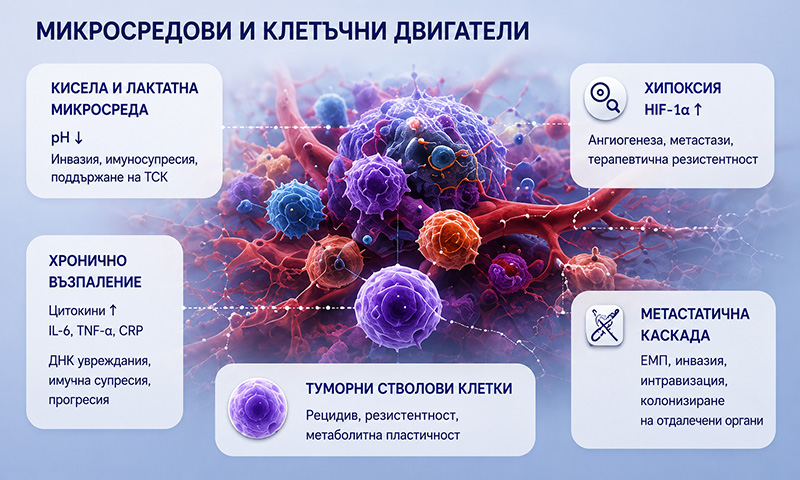
Микросредови и клетъчни двигатели на прогресията
Докато вътрешните метаболитни и сигнални пътища захранват оцеляването на раковите клетки, туморната прогресия се определя в еднаква степен от заобикалящата микросреда. Фактори като стволоподобни субпопулации, метастатична компетентност, извънклетъчна киселинност и хронично възпаление създават условия, защитаващи злокачествените клетки, позволяващи разпространението им и захранващи рецидивите.
Туморни стволови клетки
Подмножество от туморните клетки — туморните стволови клетки (ТСК) — притежават самообновяване, диференциационен потенциал и висок туморно-инициращ капацитет. ТСК показват подобрено ДНК-репариране, повишена активност на лекарствено изхвърляне и засилена резистентност към оксидативен и метаболитен стрес, правейки ги значително по-устойчиви от масовите туморни клетки. Тези клетки нерядко преживяват конвенционалната химиотерапия или лъчетерапия и могат да репопулират тумори, допринасяйки за рецидив. Клинично, высоките ТСК-сигнатури корелират с терапевтична резистентност, метастатично разпространение и лоши резултати при множество видове рак.
Метастатична каскада
Метастазите причиняват над 90% от смъртните случаи, свързани с рак. Тя е многоетапна биологична програма, обхващаща локална инвазия, епително-мезенхимен преход (ЕМП), интравазация, оцеляване в кръвообращението, екстравазация и колонизиране на отдалечени органи. Тези стъпки се поддържат от метаболитни и микросредови адаптации: гликолизата и лактатът насърчават ЕМП и инвазията, ангиогенезата осигурява съдови входни точки, а тромбоцитите предпазват циркулиращите туморни клетки от имунно разпознаване. Адхезионни медиатори като галектин-3 улесняват свързването към ендотела и насърчават метастатичното засяване.
Кисела и лактатна микросреда
Определяща характеристика на туморната микросреда е извънклетъчната ацидоза, генерирана предимно от високата гликолитична активност и лактатния износ. Кисели условия засилват инвазията чрез активиране на матрикс-разграждащи протеази и насърчаване на ЕМП. Лактат-богатите микросреди също нарушават имунното наблюдение: цитотоксичните Т-клетки и NK-клетките функционират слабо при ниско pH, докато имуносупресивни клетъчни типове като Treg и миелоидно-получените супресорни клетки (MGSК) са в преимущество. Ацидозата допълнително поддържа поддържането на ТСК и оцеляването, свързвайки директно метаболитното препрограмиране с стволовостта и рецидива.
Хронично възпаление
Хроничното възпаление е едновременно двигател и последица от туморната прогресия. Много ракови заболявания показват повишени възпалителни цитокини и системни маркери като С-реактивен протеин (СРП), корелиращи с намалена преживяемост. Възпалението насърчава ДНК увреждания, ангиогенеза, имунна супресия и ЕМП, ускорявайки по този начин злокачествената прогресия. То също допринася за образуването на преметастатични ниши чрез набиране на производни клетки от костния мозък и ремоделиране на далечни тъкани.
Туморна хипоксия (ниско кислородна микросреда)
Туморната хипоксия възниква когато бързо пролифериращите ракови клетки надхвърлят местното кислородно снабдяване. Хипоксията стабилизира HIF-1α и HIF-2α, регулиращи гени, участващи в гликолизата, ангиогенезата, метастазите и стволовостта. Хипоксичните региони развиват тежък метаболитен стрес, непоносим за нормалните клетки, но раковите клетки се адаптират чрез увеличаване на гликолитичния поток и потискане на митохондриалното дишане. Хипоксията също насърчава имунното избягване чрез намаляване на инфилтрацията на цитотоксични Т-клетки. Клинично, хипоксичните тумори са свързани с агресивно поведение, терапевтична резистентност и лоша прогноза.
Метаболитни дисфункции на гостоприемника
Раковата прогресия е силно повлияна от метаболитното състояние на гостоприемника. Системни аномалии — включително възпаление, хипергликемия, хематологичен дисбаланс, хранителни дефицити, нарушения в циркадния ритъм и по-широки метаболитни дисфункции — създават физиологични условия, насърчаващи туморния растеж и нарушаващи имунното наблюдение. Адресирането на тези дисфункции е следователно от съществено значение за всяка комплексна ЦМТ рамка.
Системно възпаление
Хроничното възпаление е тясно свързано с по-лоши резултати при онкологично болни пациенти. Повишени СРП и скорост на утаяване на еритроцитите (СУЕ) отразяват системното възпалително активиране и предсказват намалена преживяемост. Възпалението — задвижено от лоша диета, затлъстяване, заседнал начин на живот, токсини или хронични инфекции — насърчава туморния растеж чрез ангиогенеза, цитокинова сигнализация, имунна супресия и ремоделиране на извънклетъчния матрикс.
Хипергликемия и инсулинова резистентност
Хипергликемията и хиперинсулинемията установяват метаболитна среда, ускоряваща раковия растеж. Високата глюкоза директно захранва гликолизо-зависимите тумори, докато повишеният инсулин и IGF-1 активират сигналния PI3K-AKT-mTOR ос, засилвайки пролиферацията и резистентността към апоптоза. Епидемиологичните данни показват, че диабетът и инсулиновата резистентност увеличават честотата и смъртността от рак при множество злокачествени заболявания.
Анормални кръвни показатели
Хематологичните аномалии са чести при рак и отразяват системно метаболитно и възпалително смущение. Анемията допринася за вътретуморна хипоксия, засилвайки активността на HIF-1α и насърчавайки ангиогенезата и терапевтичната резистентност. Тромбоцитозата улеснява метастатичното разпространение чрез тромбоцит-медиирана защита на циркулиращите туморни клетки. Лимфопенията сигнализира за нарушена имунна компетентност и е постоянно свързана с намалена преживяемост при напреднали злокачествени заболявания.
<<< снимка 4 - Метаболитни дисфункции на гостоприемника >>>
Хранителни дефицити
Микронутриентните дефицити нерядко придружават рака и отрицателно влияят върху метаболизма на гостоприемника и имунната регулация. Недостатъчността на витамин D е свързана с по-висока честота на рак и по-лоши резултати поради ролята му в клетъчната диференциация и имунната модулация. Дефицитите на магнезий и омега-3 мастни киселини нарушават митохондриалната функция и насърчават провъзпалителното сигнализиране. Допълнителните дефицити на цинк, селен и витамини от група В намаляват антиоксидантния капацитет и ДНК-репарирането.
Нарушения на циркадния ритъм и съня
Нарушаването на циркадните ритми все повече се признава като метаболитен двигател на раковата прогресия. Мелатонинът — онкостатичен хормон, регулиращ митохондриалната функция, имунната активност и оксидативния баланс — нерядко е потиснат при лица с лош сън или нередовни графици. Хроничните нарушения на съня повишават кортизола и възпалителните маркери, създавайки физиологичен пейзаж, благоприятстващ туморното оцеляване.
Мускулно изтощение / Ракова кахексия
Раковата кахексия е мултифакторен метаболитен синдром, характеризиращ се с продължаваща загуба на скелетна мускулатура (със или без загуба на мазнини), която не може да бъде напълно обърната от конвенционалната хранителна подкрепа. Тя произтича от същата системна възпалителна среда, движеща туморната прогресия: повишени цитокини като IL-6 и TNF-α, хронично активиране на вродения имунитет и персистиращи отговори на острата фаза. Тези възпалителни мрежи насърчават протеолизата и липолизата, нарушават анаболното сигнализиране и увеличават разхода на енергия в покой, водейки до прогресивна слабост, непоносимост към лечение и по-лоша преживяемост.
Стратегии за ЦМТ
Ефективното управление на рака изисква интервенции, които едновременно таргетират туморно-вътрешните пътища, нарушават микросредовите двигатели на прогресията и коригират системните метаболитни дисфункции при гостоприемника. ЦМТ интегрира диетични стратегии, преназначени лекарства, нутрицевтици и допълнителни метаболитни терапии за създаване на координиран, многопосочен натиск срещу злокачествения растеж.

Диетични подходи и гладуване
Кетогенна диета (КД)
Кетогенната диета ограничава въглехидратите и насочва клетъчния метаболизъм към окисляване на мастни киселини и производство на кетонни тела. Това метаболитно състояние понижава циркулиращата глюкоза и инсулина, намалявайки активирането на инсулин/IGF-1-PI3K-AKT-mTOR сигнализирането — централен двигател на раковата пролиферация. Предклиничните проучвания демонстрират забавен туморен растеж и подобрен терапевтичен отговор при кетогенни условия поради намален IGF-1, по-ниско възпаление и повишен оксидативен стрес в раковите клетки. Ранните клинични данни при глиобластом и други ракови заболявания показват осъществимост и метаболитни ползи, въпреки че мащабни изпитвания все още продължават.
Интермитентно гладуване (ИГ)
Интермитентното гладуване редува периоди на хранене и гладуване, насърчавайки метаболитното превключване от глюкоза към мастни киселини и кетони. Гладуването понижава нивата на глюкоза, инсулин и IGF-1, активирайки автофагия и пътища за клетъчна стрес-адаптация. Експерименталните доказателства показват, че ИГ сенсибилизира туморите към химиотерапевтичен и лъчетерапевтичен стрес, като защитава нормалните тъкани чрез диференциална стрес-резистентност. Малки клинични проучвания докладват намалена токсичност, свързана с лечението, и подобрена поносимост при пациенти, практикуващи структурирани протоколи на гладуване.
Продължително гладуване и диети, имитиращи гладуване
Продължителното гладуване (обикновено 48-72 часа) индуцира по-дълбока метаболитна промяна от ИГ, с маркирани намаления на циркулиращата глюкоза, инсулин и IGF-1 и едновременно нарастване на кетонните тела. Това състояние активира пътищата за клетъчен стрес-отговор и автофагия, потискайки про-растежното сигнализиране и създавайки условия, при които нормалните клетки стават по-стрес-резистентни, докато раковите клетки остават уязвими за увреждане. В предклинични модели циклите на продължително гладуване осигуряват диференциална стрес-резистентност, защитавайки здравите тъкани и засилвайки цитотоксичността на химиотерапията срещу туморите.
Преназначени лекарства за ЦМТ
Преназначените лекарства формират важен компонент на ЦМТ чрез таргетиране на ключови сигнални и метаболитни пътища, поддържащи туморния растеж. Много лекарства, първоначално разработени за паразитни, инфекциозни или метаболитни заболявания, са демонстрирали антиракови ефекти чрез механизми като инхибиране на ангиогенезата, нарушаване на митозата, модулация на имунните отговори и потискане на онкогенното сигнализиране.
Ивермектин
Ивермектинът е макроциклична лактона, широко използвана като антипаразитно средство, сега признато за многоцелева антиракова активност. Той инхибира Wnt/β-катенин и YAP/Hippo сигнализирането — ключови регулатори на поддържането на ТСК — намалявайки по този начин стволовостта и туморно-инициращия капацитет. Ивермектинът също задейства митохондриална дисфункция и натрупване на реактивни кислородни видове (РКВ), водейки до апоптоза и арест на клетъчния цикъл.
Бензимидазоли — фенбендазол и мебендазол
Фенбендазолът и мебендазолът са бензимидазолови антихелминтици, традиционно използвани за лечение на паразитни инфекции. Тяхната антиракова активност произтича от силното свързване с β-тубулин, инхибирайки полимеризацията на микротубулите и нарушавайки митозата. Това също нарушава поемането на глюкоза чрез интерференция с микротубул-зависимия GLUT трафик. Мебендазолът допълнително потиска ангиогенезата чрез намаляване на VEGF сигнализирането. Доклади за случаи и наблюдателни проучвания документират туморна регресия или стабилизиране при глиобластом, рак на дебелото черво и бял дроб.
Итраконазол
Итраконазолът е триазолово антифунгално лекарство, демонстриращо потентни антиракови ефекти чрез съдови и сигнални пътища на развитие. Той инхибира ангиогенезата чрез потискане на VEGFR сигнализирането и ендотелната пролиферация. Допълнително, итраконазолът блокира активирането на Hedgehog пътя — двигател на туморния растеж, стволовостта и хеморезистентността. В клинични условия итраконазолът е показал стабилизиране на заболяването при пациенти с рак на простатата и белия дроб, когато се използва като допълнителна терапия.
Метформин
Метформинът е орален бигуанид, използван глобално като първа линия лечение на захарен диабет тип 2. Неговата антиракова ефикасност произтича от активирането на AMPK, водещо до надолу по веригата инхибиране на mTOR пътя и потискане на анаболния метаболизъм, необходим за туморната пролиферация. Мащабни епидемиологични анализи показват, че диабетните пациенти на метформин имат намалена честота на рак и подобрена преживяемост в сравнение с тези на други глюкозо-понижаващи лекарства.
Налтрексон в ниска доза (ННД)
Налтрексонът е антагонист на опиоидните рецептори, традиционно предписван при зависимости; в ниски дози (1-4,5 mg) проявява антиракови имуномодулаторни ефекти. ННД транзиторно блокира опиоидните рецептори, произвеждайки рикошетно увеличение на ендогенните опиоиди и активирайки OGF-OGFr оста, която забавя туморната клетъчна пролиферация. Той също намалява TLR4/NF-κB-медиираното възпалително сигнализиране, понижавайки производството на цитокини и подкрепяйки антитуморната имунна активност.
Бебешки аспирин
Аспиринът в ниска доза (75-100 mg/ден) се използва широко за сърдечно-съдова профилактика поради неговата антитромбоцитна активност чрез необратимо инхибиране на COX-1. Неговото антиракова значимост произтича от намаляването на тромбоцитното активиране и предотвратяването на тромбоцитното обвиване на циркулиращи туморни клетки — критичен улесняващ фактор за метастатично разпространение. Аспиринът също потиска COX-2-производния простагландин E2, намалявайки възпалението, ангиогенезата и имуносупресията. Стабилните клинични доказателства, особено при рак на дебелото черво, демонстрират намаляване на честотата, рецидивите и смъртността при дългосрочна употреба на аспирин в ниска доза.
Нутрицевтици
Нутрицевтичните съединения представляват важен допълнителен компонент на ЦМТ. Тези агенти модулират ключови биологични процеси, замесени в раковата прогресия, включително възпаление, оксидативен стрес, туморен метаболизъм и имунна регулация. За разлика от конвенционалните фармацевтици, нутрицевтиците упражняват многоцелеви биологични ефекти с благоприятни профили на безопасност.
Куркумин
Куркуминът, главният полифенол в Curcuma longa, проявява широка антиракова активност чрез потискане на NF-κB сигнализирането, намаляване на провъзпалителни цитокини и модулиране на гликолитични ензими като LDH-A и GLUT1. Той също индуцира апоптоза чрез генериране на РКВ и митохондриалните пътища. Предклиничните модели показват инхибиране при множество видове рак, а клиничните проучвания демонстрират безопасност и потенциални синергични ефекти при комбиниране с химиотерапия или лъчетерапия.
Берберин
Берберинът, изохинолинов алкалоид в видовете Berberis, активира AMPK, водейки до надолу по веригата инхибиране на mTOR пътя и потискане на гликолизата. Той намалява циркулиращата глюкоза и подобрява инсулиновата чувствителност, косвено намалявайки горивата, достъпни за туморния метаболизъм. Берберинът също индуцира апоптоза и проявява антипролиферативни ефекти в предклинични модели на рак на дебелото черво, гърдата и черния дроб.
Масло от черен кимион (тимохинон)
Тимохинонът, основното биоактивно съединение на Nigella sativa, насърчава апоптозата чрез модулиране на BCL-2 фамилните протеини и засилване на РКВ-медиираната клетъчна смърт. Той също намалява възпалителното сигнализиране, включително активирането на IL-6, TNF-α и NF-κB. Предклиничните и in vitro проучвания демонстрират инхибиране на туморния растеж, намалена ангиогенеза и засилена чувствителност към химиотерапевтични агенти.
Омега-3 мастни киселини
Ейкозапентаеновата киселина (EPA) и докозахексаеновата киселина (DHA) проявяват противовъзпалителни и антипролиферативни ефекти чрез потискане на COX-2 активността, намаляване на NF-κB активирането и промяна на мембранния липиден състав. Включването на омега-3 мастни киселини в мембраните на туморните клетки нарушава липидните плаки и засилва чувствителността към оксидативен и метаболитен стрес. Наблюдателните проучвания свързват по-високия прием на омега-3 с намалена раковата прогресия и подобрено качество на живот.
Модифициран цитрусов пектин (МЦП)
МЦП е нискомолекулна, абсорбируема форма на пектин, инхибираща галектин-3 — въглехидрат-свързващ протеин, замесен в метастазите, имунното избягване и туморно-стромалната адхезия. Предклиничната работа демонстрира намалено метастатично разпространение, засилена NK-клетъчна активност и модулация на туморната микросреда.
Лечебни гъби (β-глюкани)
Лечебни гъби като Trametes versicolor и Lentinula edodes съдържат β-глюкани, активиращи вродения имунитет чрез дендритни клетки, макрофаги и NK-клетки. Тези полизахариди засилват производството на цитокини, насърчават антитуморните имунни отговори и подобряват поносимостта към конвенционалната терапия. Рандомизирани контролирани изпитвания при рак на стомаха и гърдата показват подобрена преживяемост и намален рецидив при използване на екстракти от гъби като допълнение.
Лактоферин
Лактоферинът е желязо-свързващ гликопротеин, ограничаващ наличността на желязо за туморните клетки, потискайки по този начин пролиферацията и оксидативния метаболизъм. Той също стимулира активността на NK-клетките и макрофагите, като намалява възпалителните цитокини. Експерименталните проучвания демонстрират инхибиране на туморния растеж, намалени метастази и подобрена имунна компетентност при различни ракови модели.
Витамини и ключови минерали
Микронутриентните дефицити са чести при онкологично болни пациенти и допринасят за нарушен имунитет, метаболитна дисфункция и намалена поносимост към лечение. Няколко витамина и минерала упражняват директни или индиректни антиракови ефекти чрез подкрепа на митохондриалната функция, ДНК-репарирането, антиоксидативната защита и имунното наблюдение.
Витамин D
Витамин D притежава добре описани антиракови ефекти чрез регулация на пролиферацията, диференциацията, апоптозата и имунната модулация. Ниският серумен 25(OH)D е свързан с повишена честота и смъртност при няколко ракови заболявания, включително рак на дебелото черво, гърдата и простатата. Механистично, активирането на рецептора за витамин D (VDR) намалява провъзпалителното сигнализиране, насърчава арест на клетъчния цикъл и засилва антитуморните имунни отговори.
Цинк
Цинкът е необходим за ДНК-репарационните ензими, функцията на p53 и нормалната апоптоза. Дефицитът води до геномна нестабилност, нарушена антиоксидантна защита и дисрегулирано имунно наблюдение, всички от които благоприятстват канцерогенезата. Експерименталните и клиничните данни предполагат, че адекватният цинков статус подкрепя антитуморния имунитет — особено T-клетъчно-медиираните отговори — и може да намали риска или прогресията на определени ракови заболявания.
Селен
Селенът, чрез ролята си в глутатионовите пероксидази и другите селенопротеини, модулира оксидативния стрес, редокс сигнализирането и имунната функция. Проспективни и интервенционни проучвания показват, че адекватният или допълнен прием на селен е свързан с намален риск от няколко ракови заболявания (напр. рак на простатата, белия дроб, дебелото черво). Антираковите действия на селена включват ограничаване на РКВ-медиираното ДНК увреждане, модулация на апоптозата и засилване на имунните отговори.
Магнезий
Магнезият участва в АТФ метаболизма, ДНК-репарирането и регулирането на инсулиновата чувствителност. Епидемиологичните проучвания съобщават за обратни асоциации между диетичния прием на магнезий и риска от рак на дебелото черво и панкреаса, предполагайки защитна роля срещу туморното развитие в метаболитно стресирани стояния. Чрез стабилизиране на геномната структура, поддържане на нормалния клетъчен цикъл и подобряване на инсулиновата чувствителност, магнезият помага за противодействие на системните метаболитни условия, движещи туморната прогресия.
Допълнителни и редокс терапии
Канабидиол (CBD масло)
Канабидиолът проявява многоцелева антиракова активност, включително индукция на апоптоза, нарушаване на митохондриалното дишане и засилване на РКВ. Предклиничните данни демонстрират инхибиране на AKT/mTOR сигнализирането и потискане на метастатичното поведение при няколко туморни модела. CBD упражнява и противовъзпалителни и имуномодулаторни ефекти, които могат допълнително да нормализират туморната микросреда.
Натриев бикарбонат (сода бикарбонат)
Извънклетъчната ацидоза допринася за инвазия, имунно избягване и метастатична прогресия. Натриевият бикарбонат буферира туморната киселинност, увеличавайки pH и намалявайки метастатичното разпространение в предклинични модели. Чрез неутрализиране на лактат-задвижената подкиселяване, бикарбонатът подобрява Т-клетъчното активиране и намалява протеазо-медиираната матриксна деградация, ограничавайки по този начин инвазията и засилвайки микросредовата съвместимост за имунно наблюдение.
Хипербарна кислородна терапия (ХБКТ)
ХБКТ увеличава тъканната оксигенация, противодействайки на туморната хипоксия — основен двигател на гликолизата, ангиогенезата и терапевтичната резистентност. Чрез повишаване на кислородното напрежение, ХБКТ намалява HIF-1α активността, засилва РКВ-медиираната уязвимост на раковите клетки и подобрява перфузията в метаболитно стресирани тъкани. Предклиничните проучвания демонстрират забавена туморна прогресия и повишена терапевтична чувствителност при комбиниране на ХБКТ с метаболитни стратегии.
Оптимизиране на начина на живот
Физически упражнения като част от целенасочената метаболитна терапия (ЦМТ)
Редовните физически упражнения подобряват инсулиновата чувствителност, намаляват кръвната глюкоза на гладно, редуцират хроничното възпаление и засилват митохондриалната функция в мускулните и имунните клетки. Тези ефекти противодействат на няколко метаболитни дисфункции на гостоприемника, свързани с туморната прогресия. Наблюдателните проучвания постоянно съобщават за намален рецидив и подобрена преживяемост сред физически активните пациенти, особено при рак на гърдата и дебелото черво.
Оптимизиране на съня
Сънят поддържа интегритета на циркадния ритъм и поддържа секрецията на мелатонин — хормон с документирани онкостатични ефекти. Нарушеният сън повишава кортизола и възпалителните цитокини, нарушавайки имунната функция и създавайки про-туморна среда. Експерименталните и клиничните данни показват, че възстановяването на здравите съновни навици подобрява поносимостта към лечение и може да забави туморната прогресия.
Управление на стреса
Хроничният психологически стрес активира симпатиковото сигнализиране и повишава кортизола и катехоламините, насърчавайки ангиогенезата, имунната супресия и метаболитната дисфункция. Стресът също усилва системното възпаление, подкрепяйки туморната прогресия. Интервенции като медитация, пълноосъзнатост и дихателни практики намаляват стресовите хормони, засилват парасимпатиковия тонус и подобряват имунния баланс.
ЦМТ — Обобщение в таблици
Таблица 1 обобщава доминиращите пътища за растеж и сигнализиране, таргетирани от ЦМТ, заедно с техните роли в раковата биология и съответните ключови интервенции.
ТАБЛИЦА 1: Пътища за растеж и сигнализиране, таргетирани от ЦМТ
| Механизъм | Роля при рак | Ключови интервенции |
| Гликолиза (ефект на Варбург) | Високо глюкозно поглъщане, натрупване на лактат, имунна супресия | Кетогенна диета, интермитентно гладуване, продължително гладуване, фенбендазол, метформин, берберин, куркумин |
| Глутаминолиза | Алтернативен горивен източник, синтез на нуклеотиди, редокс-контрол | Продължително гладуване, фенбендазол, мебендазол, куркумин, берберин |
| Ангиогенеза / HIF-1α | Неоваскуларизация, хипоксична адаптация, метаболитно препрограмиране | Итраконазол, куркумин, масло от черен кимион, CBD масло, аспирин, ХБКТ |
| Апоптотична резистентност | Митохондриална защита, избягване на програмираната клетъчна смърт | Ивермектин, фенбендазол, мебендазол, куркумин, масло от черен кимион, селен, CBD масло |
| Имунно избягване | PD-L1 сигнализиране, конкуренция за хранителни вещества, лактат-медиирана супресия | Ивермектин, налтрексон в ниска доза, лечебни гъби, витамин D, омега-3, лактоферин |
| IGF-1 / PI3K-AKT-mTOR | Сигнализиране на растежни фактори, пролиферация, метаболитно активиране | Кетогенна диета, гладуване, метформин, берберин, магнезий, CBD масло |
| Wnt / β-катенин | Стволовост, терапевтична резистентност, имунно изключване | Ивермектин, итраконазол, куркумин, берберин, масло от черен кимион |
ТАБЛИЦА 2: Микросредови двигатели, таргетирани от ЦМТ
| Двигател | Роля в прогресията | Ключови интервенции |
| Туморни стволови клетки | Туморна инициация, рецидив, терапевтична резистентност, метаболитна пластичност | Ивермектин, итраконазол, фенбендазол, мебендазол, куркумин, берберин, масло от черен кимион, гладуване, метформин |
| Метастази | ЕМП, интравазация, тромбоцитно обвиване, ендотелна адхезия, колонизиране на отдалечени органи | Модифициран цитрусов пектин, ивермектин, бебешки аспирин, омега-3, куркумин, берберин, лактоферин |
| Туморна киселинност | Имунна супресия, инвазия, деградация на извънклетъчен матрикс, поддържане на ТСК | Кетогенна диета, гладуване, натриев бикарбонат, омега-3, куркумин, ХБКТ |
| Хронично възпаление | Цитокинова сигнализация, ангиогенеза, ДНК увреждания, образуване на преметастатична ниша | Омега-3, куркумин, берберин, масло от черен кимион, CBD масло, витамин D, налтрексон в ниска доза |
| Туморна хипоксия | Активиране на HIF-1/HIF-2, ангиогенеза, имунно изключване, метастази, терапевтична резистентност | ХБКТ, итраконазол, кетогенна диета, гладуване |
ТАБЛИЦА 3: Метаболитни дисфункции на гостоприемника, таргетирани от ЦМТ
| Дисфункция | Ефект върху рака | Ключови интервенции |
| Системно възпаление (СРП, СУЕ) | Задвижва освобождаването на цитокини, ангиогенеза, ДНК увреждания, имунна супресия | Омега-3, куркумин, берберин, масло от черен кимион, CBD масло, витамин D, налтрексон в ниска доза |
| Хипергликемия / Инсулинова резистентност | Захранва гликолитичните тумори, активира IGF-1/PI3K-AKT-mTOR | Кетогенна диета, интермитентно гладуване, продължително гладуване, берберин, метформин, магнезий, упражнения |
| Анормални кръвни показатели (анемия, тромбоцитоза, лимфопения) | Хипоксия, насърчаване на метастазите чрез тромбоцити, нарушен имунитет | Кетогенна диета, омега-3, бебешки аспирин, витамин D, селен, цинк, лактоферин, налтрексон в ниска доза |
| Хранителни дефицити (Вит. D, Mg, Омега-3, Zn, Se) | Отслабва имунната функция, антиоксидантна защита, ДНК-репариране, метаболитен баланс | Витамин D, магнезий, омега-3, цинк, селен |
| Нарушения на циркадния ритъм | Нисък мелатонин, висок кортизол, повишено възпаление и метаболитен стрес | Оптимизиране на съня, синхронизиране на гладуването с циркадния ритъм, витамин D, практики за намаляване на стреса, магнезий |
| Мускулно изтощение / Ракова кахексия | Загуба на мускулна маса, митохондриален спад, метаболитна неефективност, намален имунитет, лоша преживяемост | Упражнения, омега-3, лактоферин, масло от черен кимион, кетогенна диета (с достатъчно протеин) |
Ограничения при ЦМТ
Настоящият преглед има няколко ограничения, които трябва да се имат предвид при интерпретирането на предложената рамка. Повечето доказателства, поддържащи отделните компоненти на ЦМТ, произтичат от предклинични проучвания, включително in vitro клетъчни култури и in vivo животински модели, които може да не отразяват напълно биологията на човешките тумори или клиничните резултати. Клиничните доказателства за много от предложените интервенции остават ограничени до малки пилотни проучвания, наблюдателни данни или доклади за случаи, а мащабните рандомизирани контролирани изпитвания липсват за повечето обсъдени агенти.
Профилите на безопасност, оптималните диапазони на дозиране и потенциалните взаимодействия между множеството агенти, включени в протокол на ЦМТ, не са систематично оценени в клинични условия. Комбинираното използване на преназначени лекарства, нутрицевтици и диетични интервенции наред с конвенционалните онкологични лечения изисква внимателно мониторинг и индивидуализирана клинична преценка.
Рамката на ЦМТ е следователно концептуален и механистичен модел, изискващ проспективна клинична валидация преди да могат да се направят окончателни заключения относно ефикасността и безопасността. Бъдещите изследвания трябва да дадат приоритет на добре проектирани клинични изпитвания, оценяващи координирани метаболитни интервенционни протоколи като допълнения към стандартните онкологични грижи.
Заключение
Раковата прогресия произтича от взаимодействието на множество взаимосвързани механизми, включително туморно-вътрешно метаболитно пренареждане, микросредова адаптация и системна дисфункция на ниво гостоприемник, а не от единична мутация или изолиран път. Рамката, очертана в тази статия, преосмисля рака като системно метаболитно заболяване: туморите използват гликолизата, глутаминолизата, ангиогенезата, сигнализирането за оцеляване и имунното избягване, едновременно експлоатирайки кисели, хипоксични, възпалителни ниши и метаболитно компрометиран гостоприемник. Всяка стратегия, фокусирана върху една ос в изолация, е следователно вродено уязвима за излишност и избягване.
ЦМТ е предложена като интегративен, системно-ниво отговор на този проблем. По дизайн, ЦМТ не разчита на единствен ‘магически куршум’, а прилага координиран натиск на множество нива: диетични и стратегии за гладуване, ограничаващи ключови горива и растежни сигнали; преназначени лекарства, прекъсващи онкогенни пътища и пътища на стволовостта; нутрицевтици и микронутриенти, модулиращи възпалението, редокс баланса и имунната компетентност; допълнителни редокс и кислородни терапии, преоформящи туморната микросреда; и лайфстайл интервенции, възстановяващи циркадния интегритет, мускулната маса и глобалното метаболитно здраве.
ЦМТ може да се прилага наред с конвенционалните онкологични лечения — включително химиотерапия, лъчетерапия, имунотерапия и хирургия — предлагайки допълнителен слой от метаболитен натиск, допълващ, а не конкуриращ стандартните грижи.
Клинично, този подход осигурява план за изграждане на рационални, многоцелеви протоколи, а не ad hoc комбинации от метаболитни инструменти. Той позволява планове за лечение, изградени около ясни цели — като потискане на гликолизата, изчерпване на глутаминовата зависимост, нормализиране на лактата и pH, потискане на възпалителното сигнализиране, обратно развитие на кахексията и реактивиране на имунното наблюдение.
На изследователско ниво, ЦМТ предлага структурирана парадигма за проектиране на проспективни проучвания, оценяващи метаболитните интервенции не като изолирани допълнения, а като координирани програми, насочени към определени метаболитни и микросредови крайни точки. Необходима е допълнителна клинична валидация, но наличните доказателства предполагат, че систематичното таргетиране на туморния метаболизъм, микросредата и гостоприемниковата физиология паралелно има потенциала да подобри резултатите, да намали рецидивите и да промени траекторията на заболяването от неконтролирана прогресия към трайна контрол и — в отделни случаи — пълна ремисия.
Медицински екип на Dr. Biomaster
Източник: Yahia Anane, Cureus 18(5): e108373. DOI: 10.7759/cureus.108373

















