CAR-T клетъчната терапия е революцията, която превръща собственото тяло в оръжие за борба с рака.
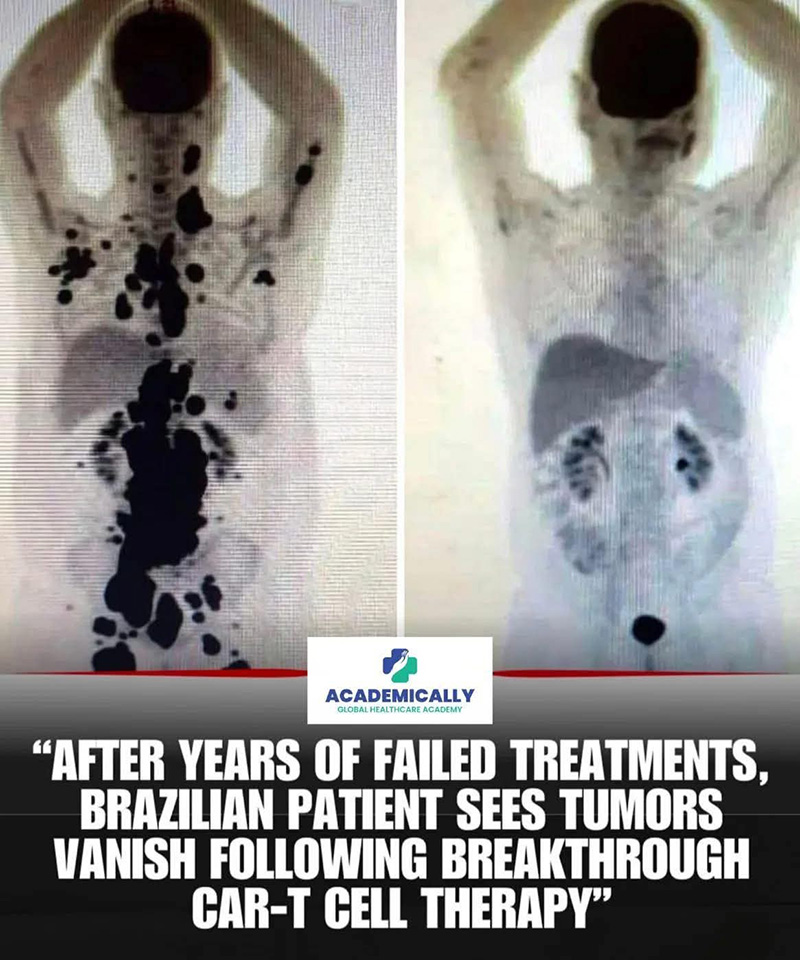
Снимките, обиколили наскоро социалните мрежи, изглеждат невероятни: ПЕТ скенер на човек показва изображение на тяло, осеяно с тъмни петна от туморни огнища, а до него — почти чист образ на същия човек, само месец по-късно. В новия ПЕТ скенер ракът сякаш е изчезнал напълно и това не е медицинска измислица. Това е историята на бразилския пациент Паоло, който е с агресивен лимфом, а в лечението му е била включена технология, която учените от Университета на Пенсилвания в САЩ нарекоха „живото лекарство — CAR-T клетъчна терапия“.
В тази статия разглеждаме как работи CAR-T клетъчната терапия, какво казват последните научни данни за нея и защо тази терапия се счита за повратна точка в историята на онкологията.
Данните до сега:
| 94% | 12+ | 7 |
| CAR-T клетъчна терапия довежда до пълна ремисия при фоликуларен лимфом при 9$% от случаите (TRANSCEND FL, 2025) | Години без рак при първия педиатричен пациент, подложен на тази терапия (2012–2024) | Броя одобрени CAR-T терапии към 2025 г. |
Какво е CAR-T клетъчна терапия?
CAR-T клетъчната терапия (от англ. „Chimeric Antigen Receptor T-cell therapy“) е персонализирана форма на имунотерапия. Тя използва собствените Т-лимфоцити на пациента — бели кръвни клетки, ключови за имунния отговор — и ги трансформира генетично, за да разпознават и унищожават раковите клетки с прецизност, невъзможна за конвенционалната химиотерапия.
„Всеки пациент получава лечение, произведено буквално от неговото собствено тяло. Това е персонализирана медицина в най-буквалния смисъл.“
— д-р Карл Юн, Университет на Пенсилвания, пионер на CAR-T терапията
Концепцията зрее от десетилетия: ако имунната система може да разпознава вируси и бактерии, защо не и рак? Проблемът е, че раковите клетки са ‘свои’ — те произлизат от нормални клетки на човешкото тяло и „имунният надзор“ на тялото ги пропуска. CAR-T терапията решава именно този проблем, като дава на Т-клетките нов ‘сенсор’ за разпознаване на тумора.
Как работи CAR-T терапията: стъпка по стъпка
- Първата стъпка се нарича Левкафереза — извличане на Т-клетки: Кръв от пациента се пропуска през специален апарат, който изолира белите кръвни клетки. Процедурата трае от 2 до 4 часа.
- Генетично инженерство — програмиране на ‘ловци’: Вирусен вектор внася в Т-клетките ген за CAR рецептор, насочен към специфичен протеин на раковите клетки (напр. CD19 при В-клетъчните лимфоми).
- Размножаване в лаборатория: Модифицираните клетки се умножават до стотици милиони в биореактори за 2 до 4 седмици. Пациентът получава лека химиотерапия през това време.
- Инфузия — връщане в тялото: CAR-T клетките се вливат интравенозно чрез единична процедура. Те намират раковите клетки и се прикрепят към тях, след което ги унищожават чрез перфорини и гранзими.
- Персистиране — ‘живото лекарство’: За разлика от химиотерапията, CAR-T клетките остават в тялото за постоянно. Изследователи от „OHSU“ (Орегонски здравен и научен университет в САЩ) са открили функционални CAR-T клетки в кръвта на пациенти повече от 5 години след инфузията.
Научните доказателства: последни данни
Фоликуларен лимфом: 94% пълна ремисия
Проучването „TRANSCEND FL“ включва 107 пациенти. Това е глобално, тригодишно клинично изпитване, оценяващо ефикасността и безопасността на lisocabtagene maraleucel (liso-cel) — т.е. CD19-насочена CAR T-клетъчна терапия при пациенти с рецидивиращ или рефрактерен фоликуларен лимфом. То беше представено пред Американското дружество по хематология („American Society of Hematology“ – ASH) през декември 2025 г. Изнесените резултати показват, че лечението с lisocabtagene maraleucel (liso-cel) постига 97% общ отговор и 94% пълна ремисия. При средно проследяване от 41,5 месеца, медианата на отговора все още не е достигната — т.е. повечето пациенти, участвали в проучването, все още остават в ремисия.
🔬 Научен факт • Журнал по клинична онкология (Journal of Clinical Oncology), 2025 г.:
Петгодишни данни при пациенти с агресивен В-клетъчен лимфом потвърждават трайни ремисии. При група с очаквана 5-годишна преживяемост под 5–10%, изследователите от Орегонски здравен и научен университет в САЩ наблюдават ясни доказателства за дълготрайна ремисия. CAR-T клетки остават открити в кръвта на пациентите над 5 години след лечението.
Допълнително „подсилени“ CAR-T клетки: следващото поколение
Изследователи от медицинския факултет Перелман в Университета Пенсилвания (САЩ) публикуват в „New England Journal of Medicine“ през 2025 г. резултати от следващо поколение ‘армирани’ CAR-T клетки (“armored CAR-T cells“) – допълнително оборудвани с цитокинови усилватели. При пациенти, неотговорили на стандартна CAR-T терапия, новото лечение редуцира рака при 81% и постига пълна ремисия при 52% от участниците — при иначе безнадежден клиничен сценарий.
Петгодишни резултати при агресивен Дифузен едроклетъчен В-клетъчен лимфом (DLBCL)
Ранните клинични проучвания на Национален институт по здравеопазване в САЩ показват, че при 43 пациенти с В-клетъчни лимфоми, 51% от пациентите са в трайна ремисия от над 3 години, а един пациент е в пълна ремисия вече над 9 години.
Бразилският опит: регулаторна рамка и резултати
Бразилия е пионер в CAR-T за Латинска Америка. Здравният регулатор там – „Agência Nacional de Vigilância Sanitária“ (ANVISA), е одобрил четири CAR-T продукта за лечение и са налице девет академични CAR-T изследвания. Националният регистър в Бразилия отчита 73% обща преживяемост при 200-дневно проследяване при пациенти с неходжкинов лимфом.
Одобрени CAR-T терапии (2025 г.)
| Препарат | Таргет | Индикация | Статус |
| Kymriah (tisagenlecleucel) | CD19 | В-ALL (В-клетъчна остра лимфобластна левкемия), DLBCL (Дифузен едроклетъчен В-клетъчен лимфом) | FDA + Европейската агенция по лекарствата |
| Yescarta (axicabtagene) | CD19 | DLBCL (Дифузен едроклетъчен В-клетъчен лимфом), FL (Фоликуларен лимфом), MCL (Мантелноклетъчен лимфом) | FDA + Европейската агенция по лекарствата |
| Breyanzi (liso-cel) | CD19 | DLBCL (Дифузен едроклетъчен В-клетъчен лимфом), FL (Фоликуларен лимфом), CLL (Хронична лимфоцитна левкемия) | FDA + Европейската агенция по лекарствата |
| Carvykti (cilta-cel) | BCMA | Множествен миелом | FDA + Европейската агенция по лекарствата |
| Tecartus (brexucabtagene) | CD19 | MCL (Мантелноклетъчният лимфом), В-ALL (В-клетъчна остра лимфобластна левкемия) | FDA + Европейската агенция по лекарствата |
Странични ефекти от CAR-T терапия и рискове
CAR-T терапията не е лишена от рискове. Основното усложнение е синдромът на цитокинова буря (CRS) — свръхактивиране на имунната система, предизвикващо висока температура и в тежки случаи – органна увреда. Лекува се с тоцилизумаб (моноклонално антитяло срещу IL-6 рецептора).
Второ важно усложнение е ICANS (имунно медиирана невротоксичност) — която включва обърканост, говорни нарушения и гърчове при пациентите. Дългосрочните странични ефекти са редки. Проучване в „HemaSphere“ (2024 г.) установява, че качеството на живот се подобрява значително 12 месеца след терапията.
Бъдещето: CAR-T терапия директно в тялото
Изследователи от Университета на Пенсилвания публикуват в списание „Наука“ (Science, юни 2025 г.) революционен подход: липидни наночастици с CAR-инструкции се инжектират директно и програмират Т-клетките in situ (директно „в тялото на пациента“) — без нужда от лабораторни процедури. При успех, CAR-T терапията може да стане достъпна амбулаторно и на цена в пъти по-евтина от досегашната цена от $350,000–$500,000 за курс, колкото струва в момента в САЩ.
„Вече не говорим само за временен (имунен) отговор. Говорим за ремисия над пет години при заболяване, считано доскоро за нелечимо в този стадий.“
— д-р Ричард Мазиарц, Онкологичен институт на Орегонския университет по здравеопазване и наука, САЩ, декември 2025 г.
Често задавани въпроси
В: Какво е CAR-T клетъчна терапия, накратко?
CAR-T терапията извлича Т-клетки от пациента, модифицира ги генетично да разпознават рака, размножава ги в лаборатория и ги влива обратно в пациента. Клетките се самовъзпроизвеждат и преследват раковите клетки продължително — затова са наречени ‘живото лекарство’.
В: При какви видове рак се прилага CAR-T терапия?
Одобрена е при В-клетъчни лимфоми (DLBCL, FL, MCL), В-клетъчна остра лимфобластна левкемия и множествен миелом. Клинични проучвания изследват приложението при солидни тумори, автоимунни болести и ХИВ.
В: Колко трайни са резултатите?
Петгодишните данни при агресивен Дифузен едроклетъчен В-клетъчен лимфом (DLBCL) показват трайна ремисия при над половината пациенти. При фоликуларен лимфом медианата на отговора при 41-месечно проследяване все още не е достигната (т.е. повечето пациенти остават в ремисия).
В: Колко струва CAR-T терапията?
Цените в САЩ варират между $350,000 и $500,000 за курс. В Европа са сходни. Очакванията са новите in vivo технологии значително да намалят цената.
В: Достъпна ли е CAR-T терапията в България?
В България CAR-T терапията все още не се прилага, но е достъпна чрез лечение в чужбина по НЗОК или чрез частно финансиране в акредитирани онкологични центрове в Германия, Австрия, Франция, Израел и Великобритания.
Автор: Медицински екип на Dr. Biomaster
⚠️ Медицинска бележка: Статията е написана въз основа на публично достъпни, рецензирани научни публикации. Решенията за лечение трябва да се вземат в консултация с квалифициран хематолог-онколог на база на индивидуалния случай. За пълен достъп до оригиналните изследвания, моля следвайте предоставените линкове в секция „Източници“ по-долу. Последна актуализация: 27 Април 2025 г.
БИБЛИОГРАФИЯ И НАУЧНИ ИЗТОЧНИЦИ
Клинични проучвания и рецензирани журнали
- Svoboda J. et al. Enhanced CAR T-Cell Therapy for Lymphoma after Previous Failure.. New England Journal of Medicine, 2025; 392(18):1824.
- Ahmed S. et al. (MD Anderson Cancer Center) TRANSCEND FL: 3-year follow-up of lisocabtagene maraleucel in follicular lymphoma.. ASH Annual Meeting Abstract, декември 2025.
- Maziarz R. et al. (OHSU Knight Cancer Institute) Five-year survival outcomes of CAR-T cell therapy in large B-cell lymphoma.. Journal of Clinical Oncology, декември 2025.
- Cappell K., Kochenderfer J. et al. (NIH/NCI) Phase I CAR T-cell therapy leads to years-long remissions in relapsed B-cell lymphoma.. Journal of Clinical Oncology, октомври 2020 (обновено 2025).
- Perthus A. et al. (CHU Pontchaillou, Rennes) Remission after CAR T-cell therapy: Do lymphoma patients recover a normal life?. HemaSphere, 2024;8(5):e72. doi:10.1002/hem3.72.
- Aghajanian H., June C. et al. (Capstan Therapeutics / UPenn) In vivo CAR T cell engineering via targeted lipid nanoparticles.. Science, юни 2025.
- Svoboda J. et al. (University of Pennsylvania / Penn Medicine) Enhanced ‘armored’ CAR T-cell therapy in B-cell lymphoma: Phase I results.. ScienceDaily / Penn Medicine News, май 2025.
Бразилски регистри и регулаторна рамка
- SBTMO/CIBMTR Brazilian Registry CAR-T cell outcomes in Brazil: implementation and results 2020–2025.. Journal of Bone Marrow Transplantation and Cellular Therapy (JBMTCT), 2025;6(1).
Прегледни статии и мета-анализи
- Rafiq S. et al. CAR-T cell therapy for cancer: current challenges and future directions.. Signal Transduction and Targeted Therapy (Nature), юли 2025.
- Sterner R., Sterner J. CAR-T cell therapy: current limitations and potential strategies.. Evolving CAR-T-Cell Therapy for Cancer Treatment: From Scientific Discovery to Cures (PMC / Molecular Therapy), 2025.
- Ahmed A. et al. CAR-engineered cell therapies: current understandings and future perspectives through 2025.. PMC / NCBI, 2025.
Официални медицински организации
- American Cancer Society CAR T-cell therapy and its side effects — patient guide.. cancer.org, актуализирано 2025.
- National Cancer Institute (NCI / NIH) CAR T cells: Engineering patients’ immune cells to treat their cancers.. cancer.gov, актуализирано 2025.
- National Institutes of Health (NIH Research Matters) Engineering immune cells within the body — lipid nanoparticle approach.. NIH, септември 2025.
- FDA — U.S. Food & Drug Administration Approved CAR-T Cell Therapy Products.. FDA.gov, актуализирано 2025.















